Als Acyloin-Kondensation bezeichnet man in der Organischen Chemie die Kondensation zweier Ester zu α-Hydroxycarbonylverbindungen (Acyloine) durch Umsetzung in der Wärme mit Natrium in Toluol oder Xylol. Die Reaktion zählt zu den Radikalreaktionen.
Übersichtsreaktion
Bei der Acyloin-Kondensation reagieren zwei Ester zu einem Acyloin:
Die Reste R1 und R2 sind Organyl-Reste. Die grüne Bindung im Acyloin ist die neu geknüpfte Verbindung zwischen den beiden Estern.
Mechanismus
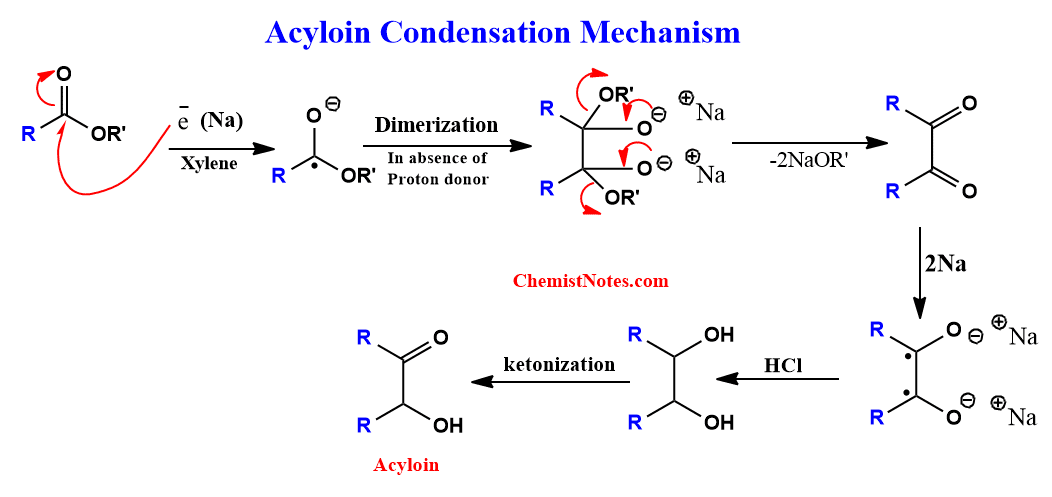
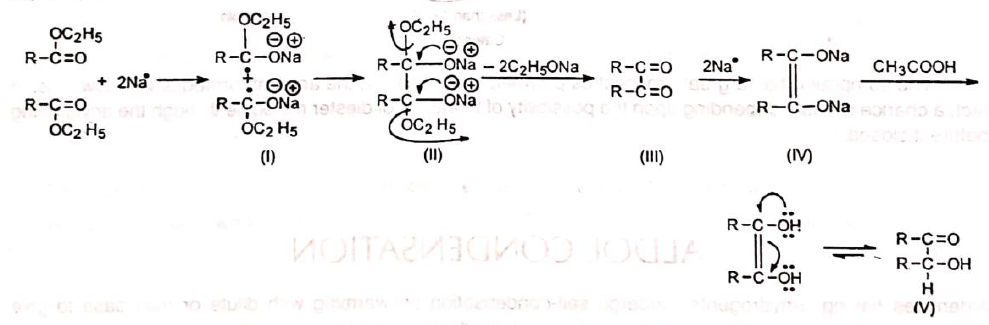
Der Mechanismus der Acyloin-Kondensation wird an dem obigen Beispiel erläutert.
Zuerst reagiert der Ester 1 mit Natrium zum Radikalanion 2, das mit einem weiteren Radikalanion zu dem Dianion 3 dimerisert. Durch Abspaltung von zwei Alkoholat-Resten (R2O−) entsteht ein Diketon 4, welches mit überschüssigem Natrium zum Dianion 5 reduziert wird. Dieses Dianion wird dann bei wässriger Aufarbeitung zum α-Hydroxyketon 6, dem Acyloin, hydrolysiert.
Rühlmann-Variante
Zur drastischen Verbesserung der Ausbeute kann Trimethylsilylchlorid (TMSCl) zugesetzt werden, das als Abfangreagenz für die basischen Alkoholate dient. Konkurrenzreaktionen werden so unterdrückt.
Durch Hydrolyse der Silylether erhält man die Acyloine.
Intramolekulare Variante
Auch die intramolekulare Variante (Prelog-Stoll-Cyclisierung) ist aus Edukten mit zwei Estergruppen möglich. Über diese Methode sind aus geeigneten Dicarbonsäurediestern entsprechende Ringsysteme zugänglich – je nach Kettenlänge des Einsatzmaterials. Die Ausbeuten für die cyclische Variante variieren in Bezug auf die Kettenlänge – einige Systeme bilden sich leichter als andere. Von präparativer Bedeutung ist vor allem die Bildung von größeren Ringen (10- oder 12-gliedrige) unter Anwendung des Ziegler-Ruggli-Verdünnungsprinzips. Die Gegenwart von Doppel- oder Dreifachbindungen im Kohlenstoffsystem stört die Reaktion im Allgemeinen nicht.
Catenane
Mittels der innermolekularen Variante lassen sich auch Catenane synthetisieren.
Literatur
- Hans Beyer, Wolfgang Walter: Lehrbuch der Organischen Chemie. S. Hirzel Verlag, Stuttgart / Leipzig 1998, 23. überarb. und aktualisierte Auflage, ISBN 3-7776-0808-4.
Einzelnachweise
Weblinks